乙醇脱氢酶的测定实验-还原反应测定
原理ADH 反应:乙醛 + NADPH + H+ ⇌ 乙醇 + NAD+此反应是可逆的,并且可以从两个位点检测出来,平衡常数是 81012 mol/L。乙醇的生
原理
ADH 反应:
乙醛 + NADPH + H+ ⇌ 乙醇 + NAD+
此反应是可逆的,并且可以从两个位点检测出来,平衡常数是 8×1012 mol/L。乙醇的生成是人们希望看到的,由此可以更为简单地检测这个方向的反应进程。但是也有极为不利的因素,即乙醛的毒性以及此反应速度过快。
材料与仪器
乙醇脱氢酶磷酸钾 BSA 溶液 NADH 乙醛
分光光度计
步骤
实验所需「试剂」具体见「其他」
0.98 ml 的实验混合物
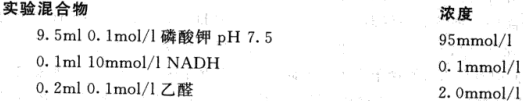
0.02 ml ADH(0.02 IU)
25 ℃ 时,于 340 nm 处吸收值降低。为了方便量化,经常使用 NADH 的吸收系数 ε340=6.3×103 l/(mol·cm)。
常见问题
试剂:
0.1 mol/L 磷酸钾,pH 7.5
0.1 g BSA 溶于 100 ml 0.1 mol/L 磷酸钾溶液中,pH 7.5(BSA 溶液)
0.01 mol/L NADH(71 mg 溶于 10 ml H2O)
0.5 mol/L 乙醛,2.2 g(2.82 ml)溶于 100 ml H2O
用 BSA 溶液稀释 ADH:按照其活性,商业购买的酶需要被稀释,例如 0.02 IU 的 ADH 每分钟转化 0.02 mol NADH,相当于吸收值变化 0.126,这是一个对反应来说很方便的数值。对于 400 IU/mg 购买的 ADH,也许需要将 10 mg/ml(4000 IU/ml)的原料溶液溶于 pH 7.5、0.1 mol/L 的磷酸钾中。然后,稀释溶液 4000 倍(2.5 ul 溶于 10 ml BSA 溶液中),使其最终为 1 IU/ml。取出 20 ul 做酶的测定实验。





