小鼠小肠类器官培养方案
一、组织提取
1. 动物房中取C57 6-8周小鼠,采用颈椎脱臼法处死后,从腹部剖开。
2. 从胃贲门后约2 cm处开始,取6-8 cm的小肠,放入含有PBS的培养皿中。
3. 小心去除小肠外壁的肠系膜。
4. 用灌胃针从小肠一端注入PBS,清洗小肠内容物,两端各重复2-3次。
5. 将小肠置于在离心管中,用含1%双抗的PBS清洗两次,每次上下颠倒震荡后更换新的PBS。
6. 在培养皿中加入含双抗的PBS,将小肠放入后,剪去两端部分,然后从中间剖开,展开后剪成约2 cm的片段。
7. 将得到的小肠片段加入含1%双抗的PBS中,剧烈震荡一次后,再缓慢震荡,不断更换PBS清洗直至溶液不再浑浊(一般重复5-6次)。清洗两次后,观察溶液中游离小肠绒毛的数目,以确定小肠的状态。
8. 取20 mL含1%双抗的PBS,加入0.1%胶原酶I和1 mM EDTA,将小肠片段放入其中,冰上消化25 min。同时取两支15 mL离心管,用1%的BSA润洗后备用。
9. 消化完成后,弃去消化液,加入新的PBS大力摇晃,以洗脱部分容易脱落的绒毛。然后更换PBS,轻轻摇晃直至溶液澄清。
10. 将盖玻片洗净,依次用ddH2O、酒精和PBS冲洗。
11. 在加有PBS的培养皿上,用盖玻片将小肠隐窝刮下,注意力度适中。
12. 用PBS将玻片上的隐窝冲到50 mL离心管中,并取样在显微镜下观察隐窝状态和大概的数目。
13. 100×g,4℃离心1 min。
14. 弃上清,用20 mL PBS重悬,并取样观察。
15. 将上一步得到的细胞悬液用经1% BSA润洗过的100 μm滤网过滤,收集滤液后,以69×g,4℃离心5 min。
二、类器官培养
1. 弃上清,用5 mL的小鼠小肠类器官培养基重悬沉淀,然后转移到15 mL离心管中,以69×g,4℃离心5 min。
2. 计数后,转至超净工作台操作,弃上清,根据沉淀量,使隐窝密度约为8-10个隐窝/μL,按3:7的比例加入培养基与基质胶(PB180536)混合液。注意在冰上操作,防止基质胶凝固,用1 mL移液枪轻轻混匀。
3. 将30 μL含有隐窝的基质胶混合液轻柔地加入预热的24孔板中,避免枪头触碰到孔板底部。
4. 将种好的24孔板置于37℃、5% CO2培养箱孵育10-20 min,使基质胶完全凝固。
5. 待基质胶凝固后,每孔加入500 μL小鼠小肠类器官完全培养基,继续在37℃、5% CO2培养箱中培养。
6. 每隔3天更换一次培养基。通常在培养5-7天后,根据类器官的生长情况,可按1:2或其他适当比例进行传代。
所用类器官培养基如下:
产品名称 | 货号 | 使用浓度 |
Advanced DMEM/F12 | PM153312 | N/A |
B-27神经细胞添加剂(50×),不含维生素A | PB180638 | 1× |
N-2 添加剂(100×) | PB180641 | 1× |
N-乙酰-L-半胱氨酸(NAC)溶液(0.5 M) | PB180601 | 1.25 mM |
R-spondin 1/RSPO1, Human, Recombinant | PCK214 | 500 ng/mL |
EGF/Urogastrone/URG, Mouse, Recombinant | PCK002 | 50 ng/mL |
Noggin/NOG (N-8His-Flag), Human, Recombinant | PCK211 | 100 ng/mL |
HEPES液(1 M) | PB180325 | 1× |
L-丙氨酰-L-谷氨酰胺溶液(GlutaMAX)(200 mM),100× | PB180419 | 1× |
青霉素-链霉素溶液(双抗),100× | PB180120 | 1× |
三、类器官传代
1. 计算与准备:首先计算胶滴中类器官的数量,每个新胶滴应包含约50-200个类器官。根据此数量,计划传代所需的胶滴数量。
2. 收集类器官:吸去培养基,加入1-2 mL左右预冷至4℃的类器官传代培养基,轻柔吹打,使基质胶充分分散。
3. 吹打分散:继续轻柔吹打,将类器官分散成较小的细胞团或碎片。
4. 洗涤:将吹打后的类器官收集至15 mL离心管中,加入Advanced DMEM/F12培养基至6-8 mL(培养基越多,基质胶被稀释得越充分,越容易去除)。
5. 离心收集:300×g,离心5 min,弃去上清,收集沉淀的类器官。
注:若类器官体积较大,难以通过吹打充分吹散,可采用消化法辅助分散。
1. 消化处理:接步骤1(计算与准备),将培养类器官的24孔板从培养箱中取出,用移液器吸去培养基。每孔加入0.5-1 mL类器官消化液,使用1 mL移液枪头轻柔吹打,使胶滴充分分散(根据类器官数量可适当增加类器官消化液的用量)。将培养板置于室温下消化5-8 min,或放入37℃培养箱中消化3-5 min。密切观察消化情况,当出现大量细胞团时即可终止消化,避免过度消化影响类器官活性和生长。
2. 类器官收集:将消化后的类器官悬液转移至含有6 mL预冷的Advanced DMEM/F12培养基的离心管中,确保培养孔中的类器官被完全收集。以300×g离心5 min,弃去上清,保留沉淀中的类器官。
3. 接种:根据类器官计数结果,将细胞沉淀重悬于基质胶中。提前将24孔板置于37℃预热至少30 min。每孔接种30 μL类器官悬液,胶滴应尽量接种于孔中央,避免接触孔壁。将接种好的培养板放置在37℃孵育10-15 min,以待基质胶完全凝固。
4. 培养与换液:待基质胶凝固后,使用移液枪沿孔壁向每孔中缓慢加入500 μL预热的胃类器官培养基,避免冲散胶滴。对于未接种类器官的孔,可加入适量PBS以保持培养环境的湿度。将培养板置于37℃、5%CO2培养箱中培养。建议每2-3 d更换一次新鲜培养基。定期观察类器官生长情况并拍照记录,直至下次传代。
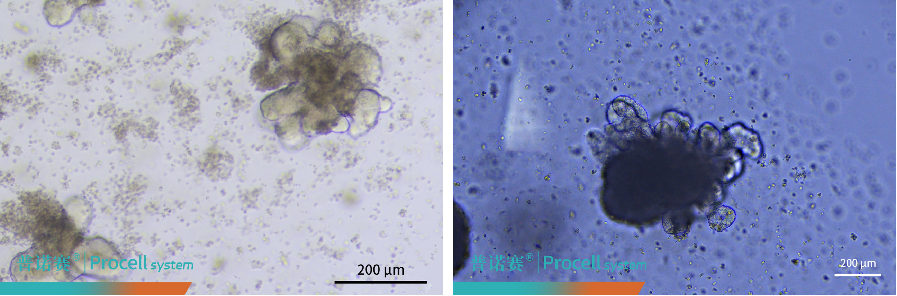
图1. 显微镜下观察不同代次小肠类器官形态(左:P0;右:P1)
四、类器官冻存
1. 类器官收集:小心吸去培养孔中的培养基,加入1-2 mL Advanced DMEM/F12培养基,轻柔吹打,使基质胶充分分散,将类器官悬液收集在15 mL离心管中。
2. 洗涤:向离心管中加入适量Advanced DMEM/F12培养基,定容至6-8 mL(培养基用量越多,基质胶被稀释得越充分,越容易去除)。
3. 离心:以300×g,离心5 min,弃上清及残留的基质胶,保留沉淀中的类器官。
4. 冻存:加入适量类器官冻存液,轻柔重悬沉淀,确保混合均匀。将重悬后的类器官分装至标记好的冻存管中,每管1 mL。将冻存管放入程序降温盒中,-80℃冰箱过夜,次日转移至液氮罐中长期保存。建议冻存密度为每1 mL约500个类器官。
五、类器官复苏
1. 从液氮罐中迅速取出冻存管,立即投入到已预热至37℃的水浴锅中解冻1-2 min,期间不断轻轻摇动,使冻存液迅速融化。
2. 将解冻后的含有类器官的冻存液转移至15 mL离心管中,加入6-8 mL类器官传代培养基重悬,轻柔吹打混匀6-8次,300×g、4℃离心5 min,弃上清。
3. 基质胶重悬类器官沉淀,轻轻混匀。将24孔板提前预热30 min,每孔加入30 μL类器官悬液,胶滴应尽量位于培养孔中央,避免接触孔壁。
4. 将接种好的培养板放置在37℃培养箱中静置10-15 min,使基质胶充分凝固。
5. 待基质胶凝固后,沿孔壁缓慢加入500 μL传代培养基,避免冲散胶滴。将培养板置于37℃、5% CO₂培养箱中进行培养。
六、小鼠小肠类器官免疫荧光鉴
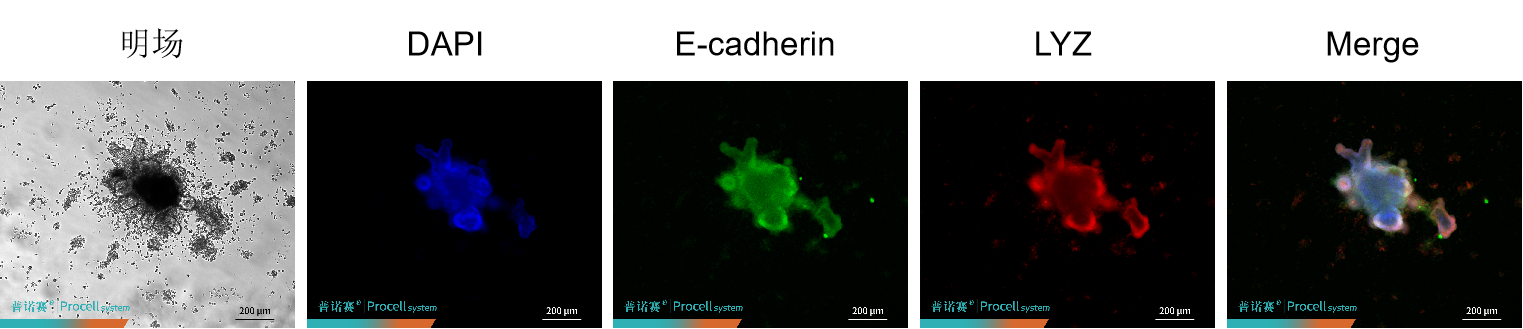
图2. 构建完成的小鼠小肠类器官免疫荧光鉴定结果图
E-cadherin在所有上皮细胞的细胞膜上连续表达,清晰地勾勒出类器官的完整结构。LYZ是潘氏细胞的特异性标志物,潘氏细胞是位于小肠隐窝底部的一种特化上皮细胞,它们通过分泌溶菌酶、防御素等抗菌肽来调节肠道菌群并保护肠道干细胞。两种标志物免疫荧光鉴定呈阳性表明小肠类器官构建成功。




