Real-time PCR(基本方法二)
材料与仪器
关于 Trizol Reagent 需要的试剂
1. Chloroform:氯仿 (分析纯)
2. Isoproplyl alcohol:异丙醇(分析纯)
3. 75% Ethanol(in DEPC-treated water):75%乙醇。要求用分析纯无水乙醇并用0.01%的DEPC处理过的无Rnase的水稀释。
4. RNase-free water:无Rnase的水。方法是:将DEPC按0.01%(V/V)加在dH2O中500 ml(50 ul),在37 ℃过夜,并高压灭菌即得(150 ℃ 3小时)
5. 一次性塑料手套
6. 注意:DEPC 致癌之嫌
7. 抽提出的细胞总 RNA 干燥后加水 50 ul,取10 ul 加无 Rnase 水 990 ul,稀释100倍成1 ml。于 0.5 cm 厚的石英比色杯中,以无Rnase水为对照,在721型紫外分光光度计下检测,结果应为:A260/280 ratio <1.6。
8. 分离组织 10 mg(纯组织)加 800 ul Trizol 试剂。
步骤
DEPC 处理方法如下
1. DEPC处理
(1)DEPC水:100 ml超纯水加入0.2 ml DEPC,充分混匀,高压灭菌。
(2) Tip头(枪头). EP管等在提RNA过程中及做RT时接触RNA的器材(包括1 ml. 200 μl. 20 μl Tip头;EP管和PCR反应管等):用0.1%的DEPC水(1000 ml超纯水加入1ml DEPC)37 ℃浸泡过夜,高压灭菌。
2. 提取RNA,用 DEPC 水溶解
3. RT 我是用PCR仪来控制温度和时间的,所以RT是在PCR反应管中作的。
4. 操作过程中要戴一次性手套,并经常换手套。 最好把要直接接触样品的东西都用DEPC水处理一下,枪头盒插好枪头后,加入1-2 ml的0.1%DEPC水,再灭菌就行了;现在有进口的 RNASE FREE 的枪头买,直接用不用处理的。
如何消除污染?
机器运行完后,取出PCR产物时不能随便丢弃,应该用塑料手套或其他打结包好后丢入垃圾桶。
(1) 试剂:mixer尽量分装,不要原瓶多次取用。
(2) 加样:原则是DNA最后加,其他试剂按照体积大小从大往小的加。如果是同种引物和探针有多管的话只是DNA不同,那么采取的方法是算出总体积后加在一个管子里面,混合均匀之后再分装到各个管子里去,这样可以有效地避免误差及污染。 另外,普通实验室容易污染,且污染程度很高,与跑电泳还有质粒制备提取都在同一个房间里有比较大的关系,最容易造成高浓度污染的就是产物的开盖和质粒的稀释。 目前,国内外各个公司提供的诊断试剂盒大多采用了UNG来防污染。Uracil-DNA N-glycosylase(UNG)尿嘧啶DNA糖基酶,来源于大肠杆菌重组克隆表达。
RNA 定量
RNA也最好至少要用电泳,一方面定量,另一方面可以看看完整性。至于用分光光度计比较不同标本之间就更不准了。 RNA的贮藏,最主要的是温度,-20不够,最好-80,液氮最保险 mRNA是不能代替蛋白水平的分析的,因为还有翻译效率和RNA降解速度的影响。
RT-PCR有两种做法
条件具备的话可用kit进行一步法进行;若条件不太好的话可分两步进行逆转录再PCR。但后来发现两步法的结果更加理想,条带特异性强且无拖尾现象,我推测是体系更加单一比较利于PCR的进行 一定要做内参的,每一次,我想。不作内参的结果是不可信的 电泳可以不一起跑,没有关系,计算的是相对表达程度,半定量和定量RT-PCR做的都是基因相对表达量,不是绝对表达量。
mRNA的分离与纯化
步骤(4)中将RNA溶液置65 ℃中温育然后冷却至室温再上样的目的有两个,一个是破坏RNA的二级结构,尤其是mRNA Poly(A+)尾处的二级结构,使Poly(A+)尾充分暴露,从而提高Poly(A+)RNA的回收率;另一个目的是能解离mRNA与rRNA的结合,否则会导致rRNA的污染。所以此步骤不能省略。
下面,我们介绍一个可以确认RNA溶液中有没有残留的RNA酶的方法:
保温试验方法很简单的,按照样品浓度,从RNA溶液中吸取两份1 000 ng的RNA加入至0.5 ml的离心管中,并且用pH7.0的Tris缓冲液补充到10 ul的总体积,然后密闭管盖。把其中一份放入70 ℃的恒温水浴中,保温1 h。另一份放置在-20 ℃冰箱中保存1 h。 时间到了之后,取出两份样本进行电泳。电泳完成后,比较两者的电泳条带。如果两者的条带一致或者无明显差别(当然,它们的条带也要符合方法2中的条件), 则说明RNA溶液中没有残留的RNA酶污染,RNA的质量很好。相反的,如果70 ℃保温的样本有明显的降解,则说明RNA溶液中有RNA酶污染。
PCR污染与对策
1. PCR扩增产物污染
这是PCR反应中最主要最常见的污染问题,所以,扩增区的仪器什么如枪头等要注意。 还有一种容易忽视,最可能造成PCR产物污染的形式是气溶胶污染;在空气与液体面摩擦时就可形成气溶胶,在操作时比较剧烈地摇动反应管,开盖时、吸样时及污染进样枪的反复吸样都可形成气溶胶而污染.据计算一个气溶胶颗粒可含48000拷贝,因而由其造成的污染是一个值得特别重视的问题。
1)标本处理区,包括扩增摸板的制备;
2)PCR扩增区,包括反应液的配制和PCR扩增;
3)产物分析区,凝胶电泳分析,产物拍照及重组克隆的制备。
各工作区要有一定的隔离,操作器材专用,要有一定的方向性。如:标本制备→PCR扩增→产物分析→产物处理。 切记:产物分析区的产物及器材不要拿到其他两个工作区。 使用一次性吸头,严禁与PCR产物分析室的吸头混用,吸头不要长时间暴露于空气中,避免气溶胶的污染; 操作多份样品时,制备反应混合液,先将dNTP、缓冲液、引物和酶混合好,然后分装,这样即可以减少操作,避免污染,又可以增加反应的精确度。
2. 反应液污染 可采用下列方法之一处理:
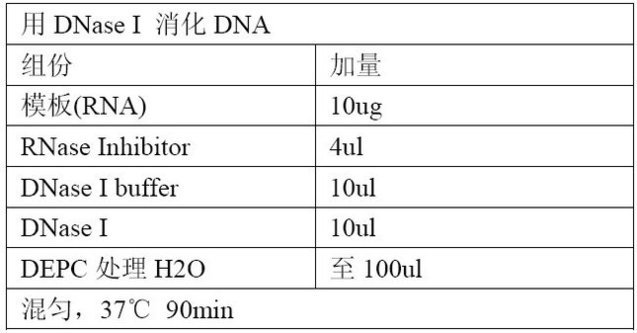
1)DNase I法:PCR混合液(未加模板和Taq聚合酶)加入0.5 U DNase I,室温反应30 min后加热灭活,然后加入模板和Taq聚合酶进行正常PCR扩增。该方法的优点是不需要知道污染DNA的序列;
2)尿嘧啶糖苷酶(UNG)法 由于UV照射的去污染作用对500 bp以下的片段效果不好,而临床用于检测的PCR扩增片段通常为300 bp左右,因此UNG的预防作用日益受到重视和肯定。
a、提取mRNA时所用的EP管、玻璃等器皿全部都要用0.1%DEPC水浸泡。然后烘干,高压灭菌,再烘干。
b、用DEPC水洗过后当然不能用双蒸水洗了。那你用DEPC处理还有什么意义呢?还要用双蒸水洗吗?
c、玻璃器皿干烤:180度,8小时或更长时间;小器皿也可以用少许氯仿处理一下。另外,铁制品、研砵等也可倒上酒精直接烧。
注意事项